


01
案例分享
02
不符合项
03
分析方法
04
整改流程
1
案例分享
不符合项案例分享
标识徽章
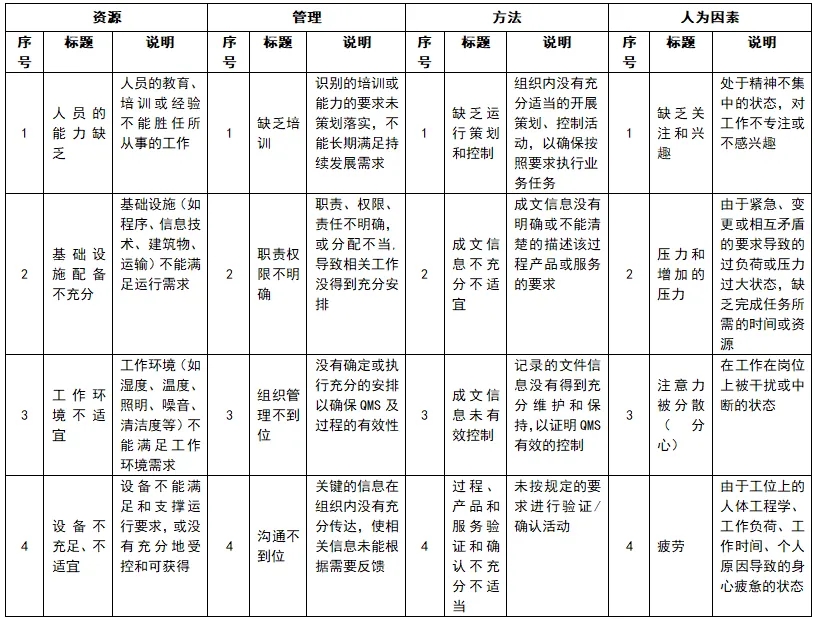
实验室地址、授权签字人、方法标准变更,未通过批准却使用了认可标识;暂停认可期间,在暂停认可的范围内使用标识等。
公正性相关
未按《质量手册》和管理程序要求提供对影响公正性的风险进行识别、评价的记录。
当影响因素有变化时,未能持续识别影响公正性的风险,如所有权/控制权变化、新进人员、新客户产生、有营销行为等。
注1:风险应包括:实验室活动、实验室的各种关系,或实验室人员的关系而引发的风险;
注2:危及实验室公正性的关系可能基于所有权、控制权、管理、人员、共享资源、财务、合同、市场营销(包括品牌推广)、给介绍新客户的人销售佣金或其他好处等。
结构
体系文件中缺少实验室活动范围的描述。或者实验室活动范围有变动,但未及时更新体系文件。
注:对实验室活动范围的描述可以在《质量手册》中规定,也可以单独形成一个文件规定。
人员
重要岗位人员实际工作职责与体系文件中的职能分配表内容不一致。
实验室未对已授权人员进行能力监控,缺乏相关记录。
注:实验室可以通过质量控制结果,包括:盲样测试、实验室内比对、能力验证和实验室间比对、现场监督实际操作过程、核查记录等方式对人员能力实施监控,做好监控记录并进行评价。
实验室未对从事以下特定活动的人员授权(无授权记录等):
①开发、修改、验证、确认方法;
②分析结果,包括符合性声明或意见和解释;
③报告、审查和批准结果。
注:实验室只用标准方法开展检测,不从事方法开发、修改,也不使用非标方法,则只需对从事方法验证的人员授权。
设备设施和
环境条件
例1:电子天平放置于无法控制温湿度、无防震措施、无防尘等条件的通风柜中/实验桌上。
注:万分之一天平不能置于空调出风口。
例2:实验室对涡轮机油样品进行固定颗粒污染度测定期间,试验区域相对湿度为30%,未控制在方法要求的40%-70%范围内。(未按方法标准要求的环境条件进行测试)
例3:实验室土壤风干和研磨处理共处一室,存在污染干扰影响。
例4:氮气瓶和高纯氮气瓶无固定装置,摆放位置不当。
计量溯源性
缺少校准结果确认和评价记录;没有校准状态标识;过期与有效标识共存;校准相关信息和内容欠缺等。
例:实验室不能提供依据GB 5009.3-2016《食品安全国家标准 食品中水分的测定》第一法检测“食品中水分”的电热恒温干燥箱的校准结果确认和评价记录。
外部提供的
产品和服务
质量体系文件中没有规定对校准服务商、能力验证提供者、设备维修维护服务商、标准物质供应商的评价要求。
注:对服务供应商可以区分为用于实验室自身活动和用于支持实验室运作。
实验室采购时忽略检测方法的要求或指标要求;实验室不能提供试剂、气体等的验收记录。
报告结果
报告结果的内容和表述不符合所依据标准的要求;报告内容缺失;报告自身信息与原始记录信息不一致等。
例1:查报告,规格型号3×0.75mm2,误为3×0.75mm;单位km误为Km(词头k大写);
例2:依据标准GB T 5023.5-2008误为GB 5023.3-2008;
例3:检测协议书中样品颜色/性状填写为“褐色软膏”,检验结果报告中样品状态填写为“均匀软膏”。
2
不符合项
不符合项:指实验室的管理或技术活动不满足要求。
要求包括:
1. CMA资质认定、CNAS认可等相关规定、要求;
2. 实验室现行有效的管理体系文件,如质量手册、程序文件、作业指导书等;
3. 检测/校准活动涉及的技术文件,如方法标准;
4. 相关法律法规,如《危险化学品安全管理条例》《中华人民共和国计量法》等。
不符合项
严重不符合项:指影响实验室诚信或技术能力,检测或校准结果准确性和可靠性,以及管理体系有效运作的不符合。
一般不符合项:对检测和校准结果的质量管理体系有效运作没有严重影响的、偶发的独立的不符合。
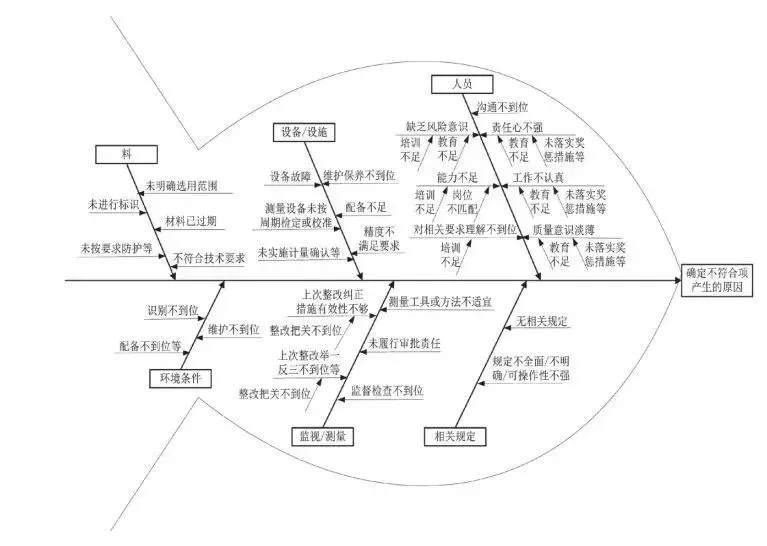
不符合项的类型
1. 实验室管理体系文件不满足CMA、CNAS等要求;
2. 体系运作不满足自身体系文件的要求;
3. 实验室缺乏必要的资源,如设备、人员等;
4. 测量溯源性不满足要求;
5. 人员能力不足以胜任所承担的工作;违规操作;
6. 操作程序,包括检测/校准的方法,缺乏技术有效性;
7. 未实施有效的质量控制活动;
8. 体系运行或活动的实施记录缺失,无法追溯等。
3
分析方法
整改不符合项的
方法介绍(原因分析)
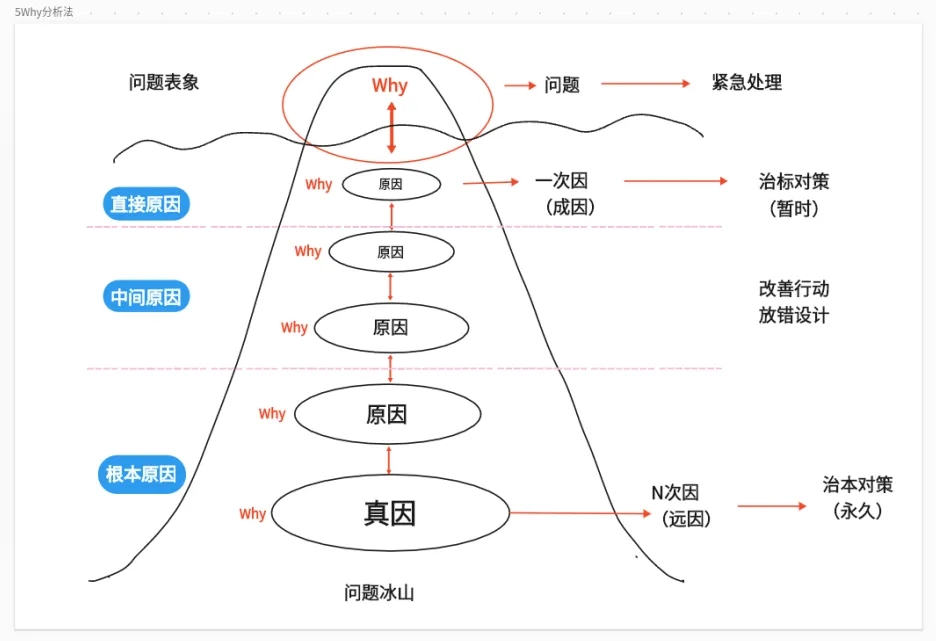
5why
“5why”分析方法即针对一个不符合,多问些“为什么”,列出所有可能的原因,然后再一一排除非根本原因,最终剩下的便是导致不符合项的根本原因。
5M1E
5M,即人(Man)、机(Machine)、料(Material)、法(Method)、测(Measurement);
1E,是环(Environment);
“测”并不是指“检测”、“测量”,而是对“结果数据”进行的质量监督、控制和评价。
人(人员)
人员能力是否适合指定工作;
人员是否经过培训;
是否建有严格的奖励和处罚制度;
工作时间与人体生物钟关系;
人员配置结构是否合理;
人员操作等熟练程度如何;
人员的质量意识和风险意识如何......
机(仪器设备)
精度够不够;
是否适应标准、规范的要求;
操作难易程度;
可靠性和稳定性如何......
料(物料材料)
样品是否适合检验;
消耗品是否经过入库检验;
材料是否还在有效期内......
法(方法标准)
是否按照标准要求的方法进行抽样并记录;
是否按标准的要求处置样品;
检验方法是否适合预期的要求;
现有的条件能否满足标准的要求......
环(环境)
实验室温湿度是否符合标准要求;
有无粉尘、噪声、电磁场和振动等的影响;
照明是否符合要求......
测(监测控制)
能力;培训;奖罚制度;人员配置;质量意识和风险意识如何等。
PDCA
PDCA,即计划、执行、检查、处理。是整改的运行原则。
4
整改流程
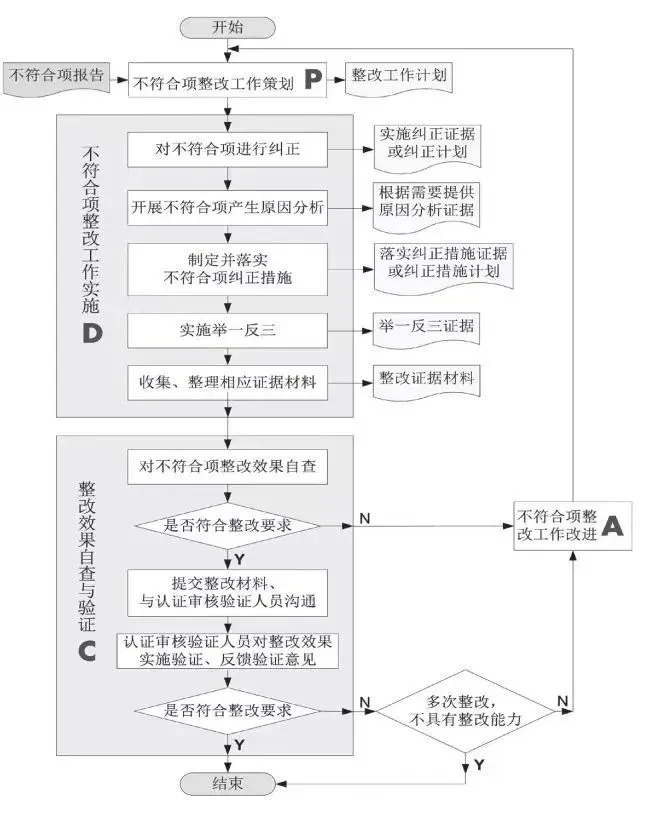
整改流程
原因分析→纠正→纠正措施→举一反三→评审验证
纠正
对于不符合项本身进行处理、为已发现的不合格采取措施。
注:针对有些无法纠正的不符合项,应将采取纠正措施后执行情况作为纠正。
例1:现场操作人员未按规定佩戴安全防护用品的立即按规定佩戴;
例2:不符合项事实对某项合同没有进行评审,但该项合同已履行完成无法纠正,对新签订的合同已按要求进行了评审(视为纠正),在无合同时可直接说明。
纠正措施
为消除已发现的不合格或其他不期望情况的原因所采取的措施,一般是针对导致不符合项的根本原因分析提出。
事后防范:为了防止再发生
事前防范:采取预防措施
1.制定纠正措施计划,针对原因采取对应的纠正措施;
2.实施纠正措施,控制纠正措施的执行情况;
3.验证纠正措施计划适宜性、有效性(需要证实性材料、记录、证据)。
注:纠正同理
举一反三
在类似产品、类似过程、其他实验室/部门中横向展开,检查是否有类似问题发生,或其他问题,一并整改。
注意事项
协助
需要其他部门进行相关工作的配合。
有效性
涉及体系文件修改、调整的,是否已经有效执行。
时限
是否有时限要求;以及注意超期处理措施。
未完成的情况
没有完成或无法完成的,需提交实验室管理者进行决策。